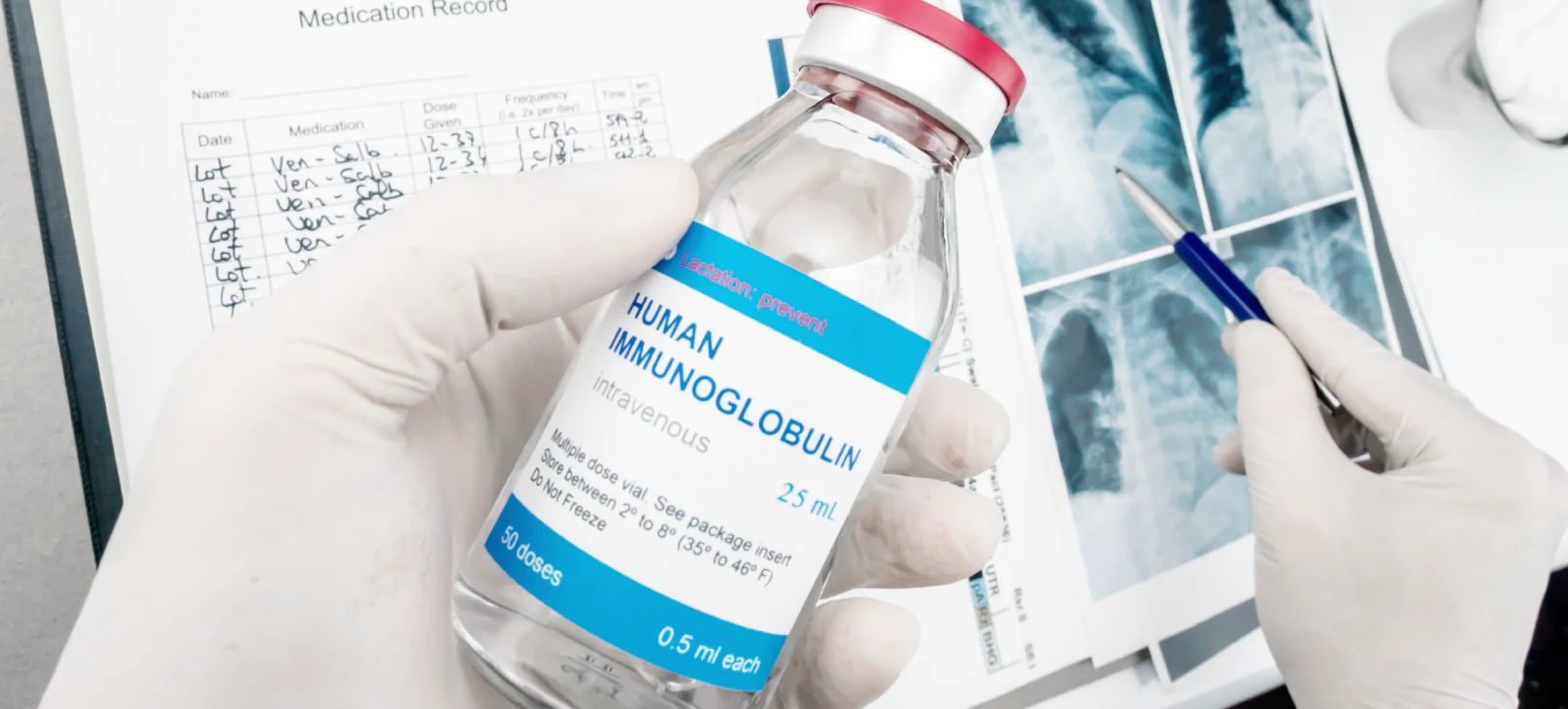
A importação excepcional de imunoglobulina humana, passou a valer após a edição da Resolução da Diretoria Colegiada – RDC nº 563, de 15 de setembro de 2021, no contexto da declaração de Emergência em Saúde Pública de Importância Internacional (ESPII) pela Organização Mundial de Saúde (OMS) e também da declaração de Emergência em Saúde Pública de Importância Nacional (ESPIN) pelo Ministério da Saúde, devido à pandemia de Covid-19.
A medida foi tomada após a constatação da iminência de desabastecimento de medicamentos à base de imunoglobulina no Brasil.
Porém, no dia 30 de junho de 2022, a Diretoria Colegiada da Agência Nacional de Vigilância Sanitária (Anvisa) aprovou a prorrogação das regras específicas para a importação excepcional e temporária do produto até o dia 31 de julho/22.
Quer saber mais? Confira este conteúdo completo que preparamos para você.
Tenha uma ótima leitura!
Imunoglobulina Humana: Para que serve?
Antes de falarmos sobre a prorrogação da importação excepcional da imunoglobulina humana, vamos entender para que serve a sua utilização.
O medicamento é usado para controlar desordens imunológicas e inflamatórias específicas, como por exemplo:
- Púrpura trombocitopênica idiopática (PTI);
- Síndrome de Kawasaki;
- Síndrome de Guillain-Barré.
Além destas patologias, a imunoglobulina humana também pode ser utilizada em terapias combinadas com antibióticos ou antivirais indicados para atuar na prevenção ou modificação aguda de infecções bacterianas e virais graves.
Leia também: Capatazia: Valor passa a ser excluído do imposto de importação
Risco de desabastecimento no Brasil
A indústria farmacêutica vem passando por situações desafiadoras como a alta demanda de medicamentos principalmente após a explosão de enfermidades causadas pelo novo SarS-Cov-2.
Embora a situação da pandemia esteja em um nível mais controlado no Brasil, o cenário continua incerto nas farmácias, inclusive nas farmácias hospitalares, que vivenciam a falta de medicamentos básicos injetáveis.
Leia também: Rastreabilidade de medicamentos: Entenda o seu papel na indústria farmacêutica
Um dos principais motivos é a volta dos surtos de Covid na China, que provocou novo lockdown e fechamento do seu Porto. O país é o principal fornecedor de matéria-prima para a produção de medicamentos.
RDC nº 563, de 15 de setembro de 2021
A Resolução da Diretoria Colegiada – RDC nº 563, de 15 de setembro de 2021, dispõe de forma temporária e extraordinária, sobre os requisitos para a importação e uso de imunoglobulina humana, devido à emergência de saúde pública internacional relacionada à Covid-19.
De acordo com o seu Art 2º, a importação em caráter excepcional e temporária, da imunoglobulina humana que não possua registro sanitário no Brasil pelo Ministério da Saúde, Secretarias Estaduais e Municipais de Saúde e por unidades de saúde, pode ocorrer desde que respeitados e atendidos os requisitos estabelecidos pela Resolução.
Entre os critérios exigidos pela medida e que deverão ser cumpridos, estão:
- Realização do peticionamento eletrônico de importação;
- Descrição da mercadoria na licença de importação contendo a inscrição “Autorizada conforme a Resolução de Diretoria Colegiada – Nº 563, de 15 de setembro de 2021”;
- Emissão do laudo de controle de qualidade da matéria-prima ativa, do produto terminado e, quando existir, do diluente, pelo fabricante;
- Conhecimento da carga embarcada;
- Licença de importação (LI) registrado no SISCOMEX;
- Autorização de funcionamento (AFE) do importador, quando couber;
- Comprovante de registro válido em país cuja autoridade regulatória competente seja membro do Conselho Internacional para Harmonização de Requisitos Técnicos de Produtos Farmacêuticos de Uso Humano (International Council for Harmonisation of Technical Requirements for Pharmaceuticals for Human Use – ICH), ou de registro válido emitido por uma das autoridades sanitárias internacionais elencadas no art. 16 da Lei nº 14.124, de 10 de março de 2021;
- Comprovante de cumprimento de boas práticas de fabricação, ou documento equivalente, do país;
- Declaração que ateste a adoção das estratégias de monitoramento e cumprimento das diretrizes de farmacovigilância;
- Declaração atestando tratar-se de importação de medicamento essencial, regularizado em autoridade sanitária estrangeira e autorizado à distribuição em seu respectivo país;
- Fatura comercial.
Confira os demais critérios exigidos acessando a RDC nº 563, de 15 de setembro de 2021 na íntegra, clicando aqui.
Leia também: Imposto de importação: Governo reduz cobrança da taxa para medicamentos
Prorrogação das regras para importação excepcional até 31 de julho

Com o objetivo de ampliar a possibilidade de importação excepcional da imunoglobulina, a medida foi prorrogada por mais 30 dias, tendo sua vigência válida até 31 de julho de 2022.
De acordo com a Anvisa, o motivo refere-se à tentativa de equilibrar as distorções do mercado e aguardar que o abastecimento alcance um nível de regularidade a partir do ajuste nos preços, por meio da disponibilização de produtos registrados no país.
A Resolução CM-CMED nº 7, de 01/06/2022 – referente à medicamentos com risco de desabastecimento, dispõe sobre a liberação dos critérios de estabelecimento ou de ajuste de preços de medicamentos com risco de desabastecimento no Brasil.
Sendo assim, visando equilibrar a oferta e a demanda por imunoglobulina humana e reconhecendo o potencial da CM-CMED nº7, de 01/06/2022, a Diretoria Colegiada aprovou a prorrogação por mais 30 dias estimando que este seja o tempo mínimo para a regularização do mercado com o fornecimento de produtos registrados.
*Com informações da Agência Nacional de Vigilância Sanitária (Anvisa).
Gostou do conteúdo? Compartilhe em suas redes sociais!